CONTENIDO
Introducción
Objetivos
Marco teórico
Conclusión
Web grafía
Evidencias
INTRODUCCIÓN
La química es la ciencia que se dedica al estudio de la estructura, las propiedades, la composición y la transformación de la materia. A grandes rasgos la química se divide en dos grupos bien definidos, la química orgánica y la química inorgánica.
Se suele clasificar los compuestos inorgánicos según su función en ácidos, bases y sales. Estos cumplen un papel importante dentro del ecosistema, cada uno posee distintas características las cuales conocerlas será de gran utilidad.
OBJETIVOS
El objetivo es conocer e identificar las distintas funciones y características que cumplen las sales, bases y ácidos dentro de los ecosistemas, sus clasificaciones, la química inorgánica, al igual que aprender donde encontrarlos, y saber si son buenos o malos.
OBJETIVOS ESPECÍFICOS:
* Clasificación de los elementos dentro de la química
* Las funciones de cada uno de ellos en el ecosistema
* Conocer sus distintas reacciones en nosotros o en lo que conocemos
MARCO TEÓRICO
La química inorgánica estudia los compuestos y los elementos inorgánicos, que no tienen enlaces de carbono. Los expertos en la materia, por lo tanto, estudian la estructura, el desarrollo y las reacciones de esta clase de sustancias. La química inorgánica forma parte de nuestra vida cotidiana mucho más de lo que podemos imaginar si somos ajenos al ámbito de la ciencia; desde productos de limpieza hasta los metales que se utilizan para fabricar los artículos más populares del mercado, esta rama de la química ocupa un sitio fundamental para la mayoría de las personas.
Dentro de la química inorgánica encontramos las sales, bases y ácidos:
Una sal es un compuesto químico formado por cationes (iones con carga positiva) enlazados a aniones (iones con carga negativa) mediante un enlace iónico. Son el producto típico de una reacción química entre una base y un ácido, donde la base proporciona el catión y el ácido el anión.
NOMENCLATURA
Según la nomenclatura tradicional, las sales se denominan con el nombre del anión, con cierto prefijo y sufijo, seguido de la preposición de y el nombre del catión. Hay que distinguir entre distintos casos:
En las sales de hidrácidos, se sustituye la terminación -hídrico del hidrácido del que proviene el anión para la terminación -uro. Por ejemplo, NaCl es el cloruro de sodio; el anión Cl- proviene del hidrácido HCl (ácido clorhídrico).
En las sales de oxoácidos, se sustituye la terminación -oso o-ico del oxoácido del cual proviene el anión por la correspondiente - ito o -ato. Por ejemplo, el Ca3(PO4)2 es el fosfato de calcio; el anión PO43- proviene del H3PO4 (ácido fosfórico).
Las sales ácidas (sales que provienen de ácidos polipróticos y que contienen átomos de hidrógeno sustituibles) se denominan indicando el número de hidrógenos no sustituidos que quedan en la molécula, usando el prefijo correspondiente. Por ejemplo, el NaHS es la hiposulfuroso de sodio; el anión HS- proviene del ácido sulfhídrico.
Las sales básicas (sales que contienen iones hidroxilo, OH-) se nombran indicando el número de hidroxilos seguido del anión central y finalmente el catión. Por ejemplo, el MgCl (OH) es el hidrocloruro de magnesio.
Las sales hidratadas (que contienen agua de cristalización) se denominan indicando la sal correspondiente y seguidamente el número de moléculas de agua de hidratación.
PROPIEDADES
Propiedades físicas: En general, las sales son materiales cristalinos con estructura iónica. Por ejemplo, los cristales de haluros de los metales alcalinos y alcalino térreos (NaCl, CsCl, CaF2) formados por aniones, situados al principio del empaquetamiento esférico más denso, y cationes que ocupan huecos dentro del paquete. Cristales de sal iónicos pueden ser también formados a partir de residuos de ácido combinados en un sinfín de estructuras dimensionales aniónicos y fragmentos de éstos con cationes en las cavidades (como los silicatos). Esta estructura se refleja apropiadamente en sus propiedades físicas: tienen altos puntos de fusión y en estado sólido son dieléctricos.
De particular interés son los líquidos iónicos, con puntos de fusión por debajo de 100 °C. Durante la fusión anormal de líquidos iónicos prácticamente no hay presión de vapor, pero si una alta viscosidad. Las propiedades especiales de estas sales se explican por la baja simetría del catión, la interacción débil entre los iones y una buena distribución de la carga del catión
COLOR: Las sales pueden tener la apariencia de ser claras y transparentes (como el cloruro de sodio), opacas e incluso metálicas y brillantes (como la pirita o sulfuro de hierro). En muchos casos la opacidad o transparencia aparentes están relacionadas con la diferencia de tamaño de los monocristales individuales; como la luz se refleja en las fronteras de grano, los cristales grandes tienden a ser transparentes, mientras que los agregados policristalinos tienen la apariencia de polvo blanco.
GUSTO: Las diferentes sales pueden provocar todos los cinco diferentes sabores básicos como, por ejemplo, el salado (cloruro de sodio), el dulce (acetato de plomo (II), que provoca saturnismo si se ingiere), el agrio (bitartrato de potasio), el amargo (sulfato de magnesio) y el umami (glutamato monosódico) .
OLOR: Las sales de ácidos fuertes y bases fuertes (sales fuertes), no suele ser volátiles y no tienen olor, mientras que las sales tanto de bases débiles como de ácidos débiles (sal débil), pueden tener olor en forma de ácido conjugado (por ejemplo, acetatos como el ácido acético o vinagre, y cianuros como el cianuro de hidrógeno en las almendras) o en forma de base conjugada (por ejemplo, sales de amonio como el amoniaco) de los iones componentes. Esta descomposición parcial y lenta es usualmente acelerada en presencia de agua, ya que la hidrólisis es la otra mitad de la ecuación de la reacción reversible de formación de las sales débiles
PROPIEDADES QUÍMICAS: Las propiedades químicas vienen determinados por las propiedades de los cationes y aniones o una parte de ellos.
Las sales reaccionan con los ácidos y las bases, obteniéndose el producto de reacción y un gas precipitado o una sustancia tal como agua; las sales reaccionan con los metales cuando éste se libera de la sal de metal en una serie electro química de reactividad; Las sales reaccionan entre sí y el producto resultante de la reacción (producen gas, y precipitan sedimentos o agua); estas reacciones pueden tener lugar con el cambio en los estados de oxidación de los átomos reactivos; algunas sales se descomponen cuando se calientan.
CLASIFICACIÓN
Las sales se pueden clasificar en los siguientes grupos:3
Sal haloidea, hidrácida o binaria neutra: son compuestos binarios formados por un metal y un no-metal, sin ningún otro elemento. El anión siempre va a tener la terminación-uro. Ejemplos: cloruro de sodio, NaCl; cloruro de hierro (III), FeCl3; sulfuro de hierro (II), FeS.
Sal de oxácido: procede de sustituir los hidrógenos de un oxácido por cationes metálicos.
Sal oxácida, oxiácida o ternaria neutra: se sustituyen todos los hidrógenos. Ejemplo: hipoclorito de sodio, NaClO.
Sal ácida: se sustituyen parte de los hidrógenos. Ejemplo: hidrogenocarbonato de sodio o bicarbonato de sodio, NaHCO3.
Sal básica o hidroxisal: contienen iones hidróxido (OH-), además de otros aniones. Se pueden clasificar como sales o hidróxidos. Ejemplo: hidroxicarbonato de hierro (III), Fe(OH)CO3.
Sal doble: se sustituyen los hidrógenos por dos o más cationes. Ejemplo: carbonato doble de potasio y litio, KLiCO3.
Hidroxosal: sal formada a partir de un hidróxido anfótero, que reacciona como un ácido una base débil ante una base o un ácido fuerte.
Al(OH)3 + 3 Na(OH) → Al(OH)6Na3 (hexahidroxoaluminato de sodio)
Al(OH)3 + 3 HCl → AlCl3 (cloruro de aluminio) + 3 H2O
Sal mixta: contiene varios aniones. Ejemplos: clorurofluoruro de calcio, CaClF; clorurofosfato de potasio, K4ClPO4, nitratosulfato de hierro (III), Fe(NO3)SO4.
Oxisal: formada por la unión de un óxido y una sal. Ejemplos: oxinitrato de plomo (IV), PbO(NO3)2; oxicloruro de cobalto (III), CoOCl.
Sal hidratada o hidrato: sal con moléculas de agua en su estructura cristalina. Ejemplos: óxido de plomo (III) hemihidrato (o hemihidratado), PbO·½H2O; sulfato de calcio dihidrato, CaSO4·2H2O.
Como puede verse en la clasificación de arriba, tanto las sales haloideas como las sales oxácidas, son llamadas «sales neutras».
LOCALIZACIÓN
Las sales se encuentran o bien en forma de mineral como parte de las rocas (como la halita), o bien disueltas en el agua (por ejemplo, el agua de mar). Son un componente vital de los seres vivos, en los que las podemos encontrar de diferentes formas:
Disueltas dentro de los organismos en los iones que las constituyen, los cuales pueden actuar en determinados procesos biológicos:
Transmisión de los impulsos nerviosos
Contracción muscular
Síntesis y actividad de la clorofila
Transporte del oxígeno de la hemoglobina
Cofactores que ayudan a las enzimas
Formando parte de estructuras sólidas insolubles que proporcionan protección o sostenimiento (huesos, conchas...)
Asociadas a moléculas orgánicas: hay iones que son imprescindibles para la síntesis de algunas biomoléculas (como por ejemplo el yodo para las hormonas fabricadas en la glándula tiroides), o para determinadas funciones (por ejemplo, el ion fosfato asociado a lípidos forma los fosfolípidos de la membrana celular; fosfoproteínas como la caseína de la leche, la molécula de hemoglobina que contiene hierro ...)
SOLUCIONES SALINAS
Una solución salina es el resultado de la reacción de un ácido fuerte con una base fuerte. Resulta altamente ionizada y, por ello, neutra. La explicación es que los contra iones de los ácidos fuertes y las bases débiles son bastante estables, y por tanto no hidrolizan al agua. Un ejemplo sería el cloruro sódico, el bromuro de litio y otras.
Una solución salina de un ácido fuerte con una base débil es ácida. Esto es así porque, tras disociarse la sal al disolverse, la base débil tiene tendencia a captar OH-,hidróxidos que va a obtener hidrolizando el agua. Finalmente, tenemos un exceso de iones hidronio en disolución que le confieren acidez a la disolución. A más débil la base, más ácida será la disolución resultante.
Químicamente: Una solución salina de un ácido débil con una base fuerte es básica. El mecanismo es el mismo que en caso anterior: el ácido, al ser débil, tenderá a captar un protón, que debe proceder necesariamente de la hidrólisis del agua. Un ejemplo, la disolución en agua del acetato de sodio.
Comúnmente se le llama solución salina a la mezcla de sal común(NaCl) y agua, en esta mezcla la sal.
IMPORTANCIA BIOLÓGICA
Las sales químicas pueden tener varias funciones:
Función estructural: las sales sólidas forman la estructura de los minerales y las estructuras esqueléticas (externas o internas) de protección y de sostenimiento de los organismos.
Función reguladora:
Función del tampón del pH: las sales son sustancias que regulan el pH de una disolución.
Presión osmótica: la ósmosis es un fenómeno que se produce cuando hay dos disoluciones diferentes de concentraciones diferentes separadas por una membrana semipermeable que permite el paso de las sustancias de bajo peso molecular. Tiene la función de igualar las dos disoluciones de manera que tengan la misma concentración mediante el paso del disolvente.
Funciones específicas: muchas sales o sus iones son necesarios para determinados procesos biológicos como la contracción muscular, la transmisión de impulsos nerviosos, etc

Es considerado tradicionalmente como cualquier compuesto químico que, cuando se disuelve en agua, produce una solución con una actividad de catión hidronio mayor que el agua pura, esto es, un pH menor que 7. Esto se aproxima a la definición moderna de Johannes Nicolaus Brønsted y Thomas Martin Lowry, quienes definieron independientemente un ácido como un compuesto que dona un catión hidrógeno (H+) a otro compuesto (denominado base). Algunos ejemplos comunes son el ácido acético (en el vinagre), el ácido clorhídrico (en el Salfumant y los jugos gástricos), el ácido acetilsalicílico (en la aspirina), o el ácido sulfúrico (usado en baterías de automóvil). Los sistemas ácido/base se diferencian de las reacciones redox en que, en estas últimas hay un cambio en el estado de oxidación. Los ácidos pueden existir en forma de sólidos, líquidos o gases, dependiendo de la temperatura y también pueden existir como sustancias puras o en solución.
A las sustancias químicas que tienen la propiedad de un ácido se les denomina ácidas.
DEFINIDO Y CONCEPTOS
Propiedades de los ácidos:
Tienen sabor agrio como en el caso del ácido cítrico en la naranja y el limón.
Cambian el color del papel tornasol azul a rosa, el anaranjado de metilo de anaranjado a rojo y deja incolora a la fenolftaleína.
Son corrosivos.
Producen quemaduras de la piel.
Son buenos conductores de electricidad en disoluciones acuosas.
Reaccionan con metales activos formando una sal e hidrógeno.
Reaccionan con bases para formar una sal más agua.
Reaccionan con óxidos metálicos para formar una sal más agua.
Ácidos Arrhenius:
El químico sueco Svante Arrhenius fue el primero en atribuir las propiedades de acidez al hidrógeno en 1884. Un ácido de Arrhenius es una sustancia que aumenta la concentración de catión hidronio, H3O+, cuando se disuelve en agua.
En agua pura, la mayoría de moléculas existen como H2O, pero un número pequeño de moléculas están constantemente disociándose y reasociándose. El agua pura es neutra con respecto a la acidez o basicidad, debido a que la concentración de iones hidróxido es siempre igual a la concentración de iones hidronio. Una base de Arrhenius es una molécula que aumenta la concentración del ion hidróxido cuando está disuelta en agua. En química se escribe con frecuencia H+(ac) significando ion hidrógeno o protón al describir reacciones ácido-base, pero no hay evidencia suficiente de que exista en disolución acuosa el núcleo de hidrógeno libre; sí que está probada la existencia del ion hidronio, H3O+ e incluso de especies de mayor nuclearidad. Los compuestos que no tienen hidrógeno en su estructura no son considerados ácidos de Arrhenius. Tampoco son bases de Arrhenius los compuestos que no tienen OH en su estructura.
Ácidos de Brønsted-Lowry:
Aunque el concepto de Arrhenius es muy útil para describir muchas reacciones, también está un poco limitado en su alcance. En 1923, los químicos Johannes Nicolaus Brønsted y Thomas Martin Lowry reconocieron independientemente que las reacciones ácido-base involucran la transferencia de un protón. Un ácido de Brønsted-Lowry (o simplemente ácido de Brønsted) es una especie que dona un protón a una base de Brønsted-Lowry. La teoría ácido-base de Brønsted-Lowry tiene varias ventajas sobre la teoría de Arrhenius.
Ambas teorías describen fácilmente la primera reacción: el CH3COOH actúa como un ácido de Arrhenius porque actúa como fuente de H3O+ cuando está disuelto en agua, y actúa como un ácido de Brønsted al donar un protón al agua. En el segundo ejemplo, el CH3COOH sufre la misma transformación, donando un protón al amoníaco (NH3), pero no puede ser descrito usando la definición de Arrhenius de un ácido, porque la reacción no produce cationes hidronio. La teoría de Brønsted-Lowry también puede ser usada para describir compuestos moleculares, mientras que los ácidos de Arrhenius deben ser compuestos iónicos. El cloruro de hidrógeno (HCl) y amoníaco se combinan bajo varias condiciones diferentes para formar cloruro de amonio, NH4Cl. En solución acuosa, el HCl se comporta como ácido clorhídrico y existe como cationes hidronio y aniones cloruro.
Ácidos de Lewis:
Un tercer concepto fue propuesto por el físicoquímico Gilbert N. Lewis en 1923, el cual incluye reacciones con características ácido-base que no involucran una transferencia de protón. Un ácido de Lewis es una especie que acepta un par de electrones de otra especie; en otras palabras, es un aceptor de par de electrones. Las reacciones ácido-base de Brønsted son reacciones de transferencia de protones, mientras que las reacciones ácido-base de Lewis son transferencias de pares de electrones. Todos los ácidos de Brønsted son también ácidos de Lewis, pero no todos los ácidos de Lewis son ácidos de Brønsted.

En la primera reacción, un anión fluoruro, F-, cede un par electrónico al trifluoruro de boro para formar el producto tetrafluoroborato. El fluoruro "pierde" un par de electrones de valencia debido a que los electrones compartidos en el enlace B-F están ubicados en la región de espacio entre los dos núcleos atómicos y, en consecuencia, están más distantes del núcleo del fluoruro que en el anión fluoruro solitario. BF3 es un ácido de Lewis porque acepta el par de electrones del fluoruro. Esta reacción no puede ser descrita en términos de la teoría de Brønsted, debido a que no hay transferencia de protones. La segunda reacción puede ser descrita por cualquiera de las dos últimas teorías. Un protón es transferido desde un ácido de Brønsted no especificado hacia el amoníaco, una base de Brønsted; alternativamente, el amoníaco actúa como una base de Lewis y transfiere un par libre de electrones para formar un enlace con un ion hidrógeno. La especie que gana el par de electrones es el ácido de Lewis; por ejemplo, el átomo de oxígeno en H3O+ gana un par de electrones cuando uno de los enlaces H-O se rompe, y los electrones compartidos en el enlace se localizan en el oxígeno. Dependiendo del contexto, los ácidos de Lewis también pueden ser descritos como agentes reductores o como electrófilo.
La definición de Brønsted-Lowry es la definición más ampliamente usada; salvo que se especifique de otra manera, se asume que las reacciones ácido-base involucran la transferencia de un catión hidrón (H+) de un ácido a una base.
NOMENCLATURA
En el sistema de nomenclatura clásico, los ácidos son nombrados de acuerdo a sus aniones. El sufijo iónico es eliminado y es reemplazado con un nuevo sufijo (y a veces prefijo), de acuerdo con la tabla siguiente.
Sistema de nomenclatura clásico:
Prefijo Anión
Sufijo Anión
Prefijo Ácido
Sufijo Ácido
Ejemplo
per
ato
per
ácido ico
ácido perclórico (HClO4)
ato
ácido ico
ácido clórico (HClO3)
ito
ácido oso
ácido cloroso (HClO2)
hipo
ito
hipo
ácido oso
ácido hipocloroso (HClO)
uro
hidro
ácido ico
ácido clorhídrico (HCl)
En el caso particular de los oxácidos, es importante tener en cuenta variedades alotrópicas.
• Nomenclatura Sistemática: se indica mediante un prefijo (Mono, di, tri, tetra....) el números de oxígenos (terminando en “oxo”) seguido del nombre del elemento central en “ato”, indicando entre paréntesis el número de oxidación de éste y finalmente diciendo “ de hidrógeno”. Por ejemplo el ácido sulfúrico es el tetraoxosulfato (VI) de hidrógeno.
• Nomenclatura simplificada: empieza el nombre del compuesto por la palabra “ácido” seguido por el número de oxígenos terminando en “oxo” y finalmente el nombre del elemento central terminado en “ico”, indicando el número de oxidación entre paréntesis en números romanos.
CARACTERÍSTICAS QUÍMICAS
Ácidos monopróticos:
Los ácidos monopróticos son aquellos ácidos que son capaces de donar un protón por molécula durante el proceso de disociación (llamado algunas veces ionización), algunos ejemplos comunes de ácidos monopróticos en ácidos minerales incluyen al ácido clorhídrico (HCl) y el ácido nítrico (HNO3). Por otra parte, para losácidos orgánicos, el término generalmente indica la presencia de un grupo carboxilo, y algunas veces estos ácidos son conocidos como ácidos monocarboxílicos.
Ácidos polipróticos:
Los ácidos polipróticos son capaces de donar más de un protón por molécula de ácido, en contraste a los ácidos monopróticos que sólo donan un protón por molécula. Los tipos específicos de ácidos polipróticos tienen nombres más específicos, como ácido diprótico (dos protones potenciales para donar) y ácido triprótico (tres protones potenciales para donar).
Un ejemplo inorgánico de un ácido triprótico es el ácido ortofosfórico (H3PO4), generalmente llamado simplemente ácido fosfórico. Los tres protones pueden ser perdidos consecutivamente, produciendo H2PO—
4, luego HPO2-
4, y finalmente PO3-
4, el anión ortofosfato, simplemente llamado fosfato. Un ejemplo orgánico de ácido triprótico es el ácido cítrico, que puede perder consecutivamente tres protones para formar finalmente el anión citrato. Aunque las posiciones de los protones en la molécula original pueden ser equivalentes, los valores de Ka difieren puesto que es energéticamente menos favorable perder un protón si la base conjugada está cargada negativamente.
APLICACIONES DE LOS ÁCIDOS
Hay numerosos usos de los ácidos. Los ácidos son usados frecuentemente para eliminar herrumbre y otra corrosión de los metales en un proceso conocido como pickling. Pueden ser usados también como electrolitos en una batería, como el ácido sulfúrico en una batería de automóvil.
Los ácidos fuertes, el ácido sulfúrico en particular, son ampliamente usados en procesamiento de minerales. Por ejemplo, los minerales de fosfato reaccionan con ácido sulfúrico produciendo ácido fosfórico para la producción de fertilizantes, y el cinc es producido disolviendo óxido de cinc en ácido sulfúrico, purificando la solución y aplicando electrólisis.
En la industria química, los ácidos reaccionan en las reacciones de neutralización para producir sales. Por ejemplo, el ácido nítrico reacciona con el amoníaco para producir nitrato de amonio, un fertilizante. Adicionalmente, los ácidos carboxílicos pueden ser esterificados con alcoholes en presencia de ácido sulfúrico, para producir ésteres.
Los ácidos son usados como catalizadores; por ejemplo, el ácido sulfúrico es usado en grandes cantidades en el proceso de alquilación para producir gasolina. Los ácidos fuertes, como el ácido sulfúrico, fosfórico y clorhídrico, también tienen efecto en reacciones de deshidratación y condensación. Los ácidos son usados también como aditivos en bebidas y alimentos, puesto que alteran su sabor y sirven como preservantes. Por ejemplo, el ácido fosfórico es un componente de las bebidas con cola.
APLICACIONES BIOLÓGICAS
Muchas moléculas biológicamente importantes son ácidos. Los ácidos nucleicos, incluyendo al ADN y el ARN contienen el código genético que determina mucho de las características de un organismo, y es transferido de padres a vástagos. El ADN contiene el molde químico para la síntesis de las proteínas, que están hechas de subunidades de aminoácidos.
Un α-aminoácido tiene un carbono central (el carbono α o alfa) que está unido covalentemente a un grupo carboxilo (de ahí que son ácidos carboxílicos), un grupo amino, un átomo de hidrógeno, y un grupo variable. El grupo variable, también llamado grupo R o cadena lateral, determina la identidad y muchas de las propiedades de un aminoácido específico. En la glicina, el aminoácido más simple, el grupo R es un átomo de hidrógeno, pero en todos los demás aminoácidos contiene uno o más átomos de carbono unidos a hidrógeno, y puede contener otros elementos, tales como azufre, selenio, oxígeno o nitrógeno. Con excepción de la glicina, los aminoácidos presentes en la naturaleza son quirales y casi invariablemente están presentes en la configuración L. Algunos peptidoglucanos, encontrados en algunas paredes celulares bacterianas contienen pequeñas cantidades de D-aminoácidos. A pH fisiológico, típicamente alrededor de 7, existen aminoácidos libres en forma iónica, donde el grupo carboxilo ácido (-COOH) pierde un protón (-COO-) y el grupo amino básico (-NH2) gana un protón (-NH+
3). La molécula entera tienen una carga neta neutra, y es un zwitterión.
Los ácidos grasos y derivados de ácidos grasos son otro grupo de ácidos carboxílicos que juegan un rol significativo en biología. Estos contienen largas cadenas de hidrocarburo y un grupo ácido carboxílico en un extremo. La membrana celular de casi todos los organismos está hecha principalmente de unabicapa fosfolipídica, una micela de cadenas hidrofóbicas de ácidos grasos con grupos fosfato hidrofílicos.
En humanos y muchos otros animales, el ácido clorhídrico es parte del ácido gástrico segregado en el estómago para ayudar a hidrolizar a las proteínas, así como para convertir la proenzima inactiva pepsinógeno en la enzima activa pepsina. Algunos organismos producen ácidos para su defensa; por ejemplo, las hormigas producen el ácido fórmico.
El equilibrio ácido-base juega un rol crítico en la regulación de la respiración de los mamíferos. El gas oxígeno (O2) lleva a cabo la respiración celular, proceso por el cual los animales liberan la energía potencial química almacenada en los alimentos, produciendo dióxido de carbono (CO2) como producto. El oxígeno y el dióxido de carbono son intercambiados en los pulmones, y el cuerpo responde a las demandas energéticas variables ajustando la velocidad deventilación pulmonar. Por ejemplo, durante períodos de ejercitación, el cuerpo rompe rápidamente los carbohidrato almacenados, liberando CO2 al torrente sanguíneo. En soluciones acuosas como la sangre, el CO2 existe en equilibrio con ácido carbónico y el anión bicarbonato.
CO2 + H2O
 H2CO3
H2CO3  H+ + HCO3-
H+ + HCO3- Es la disminución en el pH la señal que lleva al cerebro a respirar más rápidamente y profundo, liberando el exceso de CO2 y resuministrando a las células con O2.
Las membranas celulares son generalmente impermeables a las moléculas polares, cargadas o grandes, debido a las cadenas grasas acílicas lipofílicas contenidas en su interior. Muchas moléculas biológicamente importantes, incluyendo un gran número de agentes farmacéuticos, son ácidos orgánicos débiles que pueden crusar la membrana en su forma protonada, en la forma sin carga, pero no pueden hacerlo en su forma cargada (como base conjugada). Por esta razón, la actividad de muchas drogas puede ser aumentada o disminuida por el uso de antiácidos o alimentos ácidos. Sin embargo, la forma cargada suele ser más soluble en la sangre y el citosol, ambos medios acuosos. Cuando el medio extracelular es más ácido que el pH neutro dentro de la célula, ciertos ácidos existirán en su forma neutra y serán solubles en la membrana, permitiéndoles cruzar la bicapa lipídica. Los ácidos que pierden un protón a pH intracelular existirán en su forma cargada, soluble, por lo que son capaces de difundirse a través del citosol a su objetivo. El ibuprofeno, la aspirina y la penicilina son ejemplos de drogas que son ácidos débiles.
ÁCIDOS COMUNES
Ácidos minerales o inorgánicos
Halogenuros de hidrógeno y sus soluciones acuosas: ácido clorhídrico (HCl), ácido bromhídrico (HBr), ácido yodhídrico (HI)
Oxoácidos de halógenos: ácido hipocloroso, ácido clórico, ácido perclórico, ácido peryódico y compuestos correspondientes al bromo y al yodo
Ácido fluorosulfúrico
Ácido nítrico (HNO3)
Ácido fosfórico (H3PO4)
Ácido fluoroantimónico
Ácido fluorobórico
Ácido hexafluorofosfórico
Ácido crómico (H2CrO4)
Ácidos sulfónicos
Ácido metansulfónico (ácido mesílico)
Ácido etansulfónico (ácido esílico) (EtSO3H)
Ácido bencensulfónico (ácido besílico) (PhSO3H)
Ácido toluenosulfónico (ácido tosílico) (C6H4(CH3) (SO3H))
Ácido trifluorometansulfónico (ácido tríflico)
Ácidos carboxílicos
Ácido acético
Ácido fórmico
Ácido glucónico
Ácido láctico
Ácido oxálico
Ácido tartárico
Ácidos carboxílicos vinílogos
Ácido ascórbico
Ácido de Meldrum

Es cualquier sustancia que presente propiedades alcalinas. En primera aproximación (segúnArrhenius) es cualquier sustancia que en disolución acuosa aporta iones OH− al medio. Un ejemplo claro es el hidróxido potásico, de fórmula KOH:
KOH → OH− + K+ (en disolución acuosa)
Los conceptos de base y ácido son contrapuestos. Para medir la basicidad (o alcalinidad) de un medio acuoso se utiliza el concepto de pOH, que se complementa con el de pH, de forma tal que pH + pOH = pKw, (Kw en CNPT es igual a 10−14). Por este motivo, está generalizado el uso de pH tanto para ácidos como para bases.
DEFINICIONES DE BASES
La definición inicial corresponde a la formulada en 1887 por Svante August Arrhenius.
La teoría ácido-base de Brønsted-Lowry, formulada por Brønsted y Lowry en 1923, dice que una base es aquella sustancia capaz de aceptar un protón (H+). Esta definición engloba la anterior: en el ejemplo anterior, el KOH al disociarse en disolución da iones OH−, que son los que actúan como base al poder aceptar un protón. Esta teoría también se puede aplicar en disolventes no acuosos.
Lewis en 1923 amplió aún más la definición de ácidos y bases, aunque esta teoría no tendría repercusión hasta años más tarde. Según la teoría de Lewisuna base es aquella sustancia que puede donar un par de electrones. El ion OH−, al igual que otros iones o moléculas como el NH3, H2O, etc., tienen un par de electrones no enlazantes, por lo que son bases. Todas las bases según la teoría de Arrhenius o la de Brønsted y Lowry son a su vez bases de Lewis.
Ejemplos de bases de Arrhenius: NaOH, KOH, Al(OH)3.
Ejemplos de bases de Brønsted y Lowry: NH3, S2−, HS−.
PROPIEDADES DE LAS BASES
Finalmente, según Boyle, bases son aquellas sustancias que presentan las siguientes propiedades:
Poseen un sabor amargo característico.
Sus disoluciones conducen la corriente eléctrica.
Cambian el papel tornasol rojo en azul.
La mayoría son irritantes para la piel (cáusticos) ya que disuelven la grasa cutánea. Son destructivos en distintos grados para los tejidos humanos. Los polvos, nieblas y vapores provocan irritación respiratoria, de piel, ojos, y lesiones del tabique de la nariz.
Tienen un tacto jabonoso.
Son solubles en agua (sobre todo los hidróxidos).
Reaccionan con ácidos formando sal y agua.
FORMACIÓN DE UNA BASE
Una base se forma cuando un óxido metálico reacciona con agua (hidrólisis):

igual es:
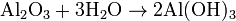
NOMENCLATURA DE BASES
Para crear una base usando diversas nomenclaturas para ellas tomadas a partir de los nombres de los elementos y juntándolos con un ion hidroxilo (OH), tomando el número de valencia del elemento y combinarlos (cambiándolos de posición) como se muestra en la tabla:
Fórmula
Tradicional
Stock
IUPAC
Cu(OH)
Hidróxido cuproso
Hidróxido de cobre (I)
Monohidróxido de cobre
Cu(OH)2
Hidróxido cúprico
Hidróxido de cobre (II)
Dihidróxido de cobre
Cuando un elemento tiene más de dos valencias no se le pone nomenclatura tradicional. Al usar la menor valencia, el elemento termina en oso y cuando se usa la mayor termina en ico. En la nomenclatura IUPAC se le va a dar una conformación de prefijos al elemento según su valencia usada (Mono, Di, Tri, Tetra, Penta, Hexa, etc) junto con la terminación -hidroxi u -oxidrilo que es el ion OH con carga −1.
EJEMPLOS DE BASES
Algunos ejemplos de bases son:
Soda cáustica (NaOH)
Leche de magnesia (Mg(OH)2)
El cloro de piscina (hipoclorito de sodio)
Antiácidos en general
Productos de limpieza
Amoníaco (NH3)
Jabón y detergente
Bicarbonato de sodio
CONCLUSIÓN
La información presentada, nos sirve para poder entender y comprender todo sobre las sales, ácidos y bases, podemos ver sobre las características , funciones y las formas en las que son presentadas de forma común al hombre, podemos ver también las distintas formas en las que son nombradas, como se forman y podemos ver pomo se reaccionan con los distintos elementos químicos.
WEB - GRAFÍA
https://es.wikipedia.org/wiki/Base_(qu%C3%ADmica)
https://es.wikipedia.org/wiki/%C3%81cido
https://es.wikipedia.org/wiki/Qu%C3%ADmica_inorg%C3%A1nica
http://definicion.de/quimica-inorganica/
https://es.wikipedia.org/wiki/Sal_(qu%C3%ADmica)
https://es.wikipedia.org/wiki/Qu%C3%ADmica
EVIDENCIAS




















No hay comentarios:
Publicar un comentario